转载:病例报告 | 子宫颈浸润性复层产黏液性癌2例
作者:于萍1 管祎琪1 王玉湘2 吴郁1 梁华茂1 郭红燕1
1北京大学第三医院妇产科, 北京 100191;2北京大学医学部基础医学院病理系 北京大学第三医院病理科, 北京 100191
通信作者:郭红燕, Email:bysyghy@163.com
引用本文:于萍,管祎琪,王玉湘,等. 子宫颈浸润性复层产黏液性癌2例[J]. 中华妇产科杂志,2025,60(07):562-565.DOI:10.3760/cma.j.cn112141-20250426-00175
摘要
子宫颈浸润性复层产黏液性癌(ISMC)是一种女性生殖系统特殊而少见、主要依赖病理检查诊断的恶性肿瘤,其常见临床表现为接触性出血及阴道不规则流血。子宫颈ISMC具有侵袭性生物学行为,恶性程度高;多为中~低分化、Silva C型;具有淋巴脉管浸润、淋巴结转移、预后差的特点,可考虑结合细胞程序性死亡配体1(PD-L1)抑制剂治疗以期得到更好的治疗效果。本文报道的2例子宫颈ISMC患者,经活检组织病理学检查确诊后行手术治疗,通过多学科团队讨论为患者制定后续治疗方案,规律随访34个月,2例患者均未复发、预后良好。本文结合文献复习,旨在提高临床和病理科医师对子宫颈ISMC的认识,有助于本病的规范诊治。
例1 患者43岁,因间断出现性交后阴道流血1个月余,于2022年7月21日在本院就诊。行液基薄层细胞学检查提示:低级别鳞状上皮内病变(low-grade squamous intraepithelial lesion,LSIL);人乳头状瘤病毒(human papillomavirus,HPV)分型检测显示,HPV 18、51型阳性。阴道镜活检后病理检查提示:子宫颈4、8、12点处HPV感染相关性腺鳞癌,绝大部分为中~低分化腺癌(复层产黏液亚型; 图1A , 2A ),少量为非角化型鳞癌。妇科检查:子宫颈糜烂、后唇略糟脆;子宫前位、正常大小、质中,活动度好,无压痛;双侧附件区未及明显异常;两侧宫旁组织未触及异常,双侧主韧带、宫骶韧带未触及增粗,直肠子宫陷凹未触及结节。考虑:子宫颈腺鳞癌Ⅰb2期可能。遂行改良的机器人系统辅助下子宫广泛性切除+双侧附件切除+盆腔淋巴清扫术。术后病理检查提示:HPV感染相关性子宫颈腺癌,为浸润性复层产黏液性癌(invasive stratified mucin-producing carcinoma,ISMC)亚型,Silva C型( 图1B , 2B ),浸润最深处位于子宫颈7点,深度约5 mm(子宫颈厚度的>1/3~<2/3处),浸润前缘可见脉管内癌栓;双侧盆腔淋巴结未见转移。免疫组化检测显示,p16、细胞角蛋白(CK)7、CK5/6阳性,细胞增殖相关核抗原(Ki-67)阳性比例约50%,p53突变型(全阴性)。见 图3 。术后诊断:子宫颈中~低分化腺癌(ISMC亚型),Ⅰb2期。经过多学科团队讨论,考虑患者的病理类型为ISMC,生物学特性为强侵袭性,依据子宫颈腺癌分型为Silva C型,存在四因素模型中危因素:腺癌、脉管内癌栓。综上,给予患者术后补充同步放化疗治疗。治疗后规律随访34个月,无复发征象。
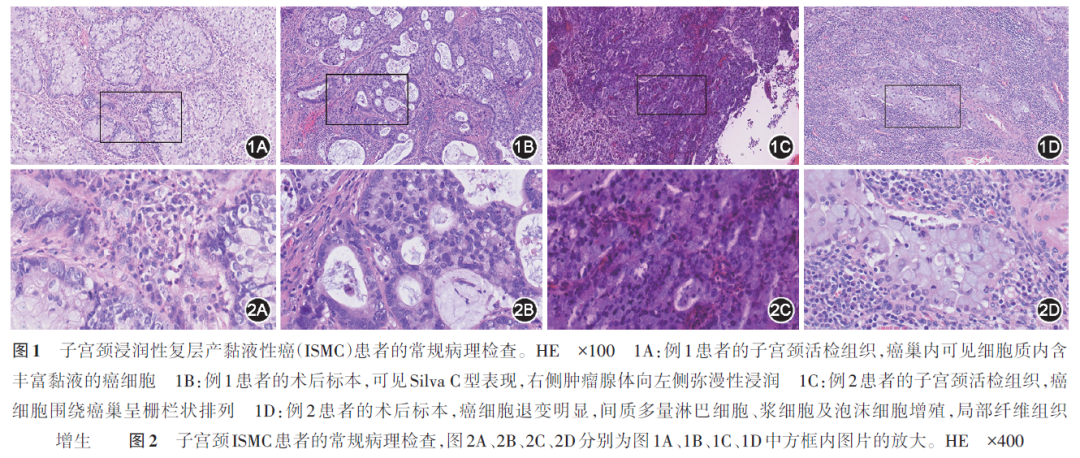
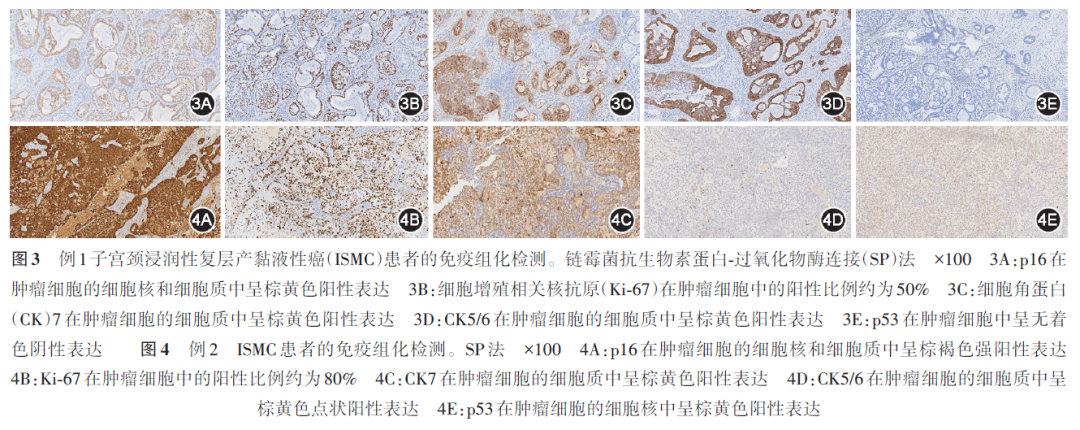
例2 患者43岁,因阴道不规则流血2年、增多1个月,于2022年7月8日在本院就诊。妇科检查:子宫颈肿物5~6 cm,质硬;子宫前位、正常大小、质中,活动度好,无压痛;双侧附件区未及明显异常;两侧宫旁组织未触及异常,双侧主韧带、宫骶韧带未触及增粗,直肠子宫陷凹未触及结节。盆腔超声检查提示:子宫颈形态失常,可探及形态不规则低回声,大小为4.5 cm×5.4 cm,其内血流信号丰富。血清鳞状上皮细胞癌抗原(SCC-Ag)水平为3.2 μg/L。盆腔增强磁共振成像(MRI)检查提示:子宫颈肿物侵犯子宫体以及阴道上2/3,伴双侧髂血管走行区多发肿大淋巴结。考虑:子宫颈癌Ⅲc1r期。活检病理检查提示:HPV感染相关性子宫颈ISMC( 图1C , 2C )。予白蛋白紫杉醇+卡铂方案静脉化疗2个疗程后,复查盆腔MRI提示病灶较前缩小,双侧髂血管旁见多发肿大淋巴结,考虑盆腔多发淋巴结转移?遂行改良的机器人系统辅助下腹腔镜子宫广泛性切除+双侧附件切除+盆腔和腹主动脉旁淋巴清扫+右侧腹股沟淋巴结切除术。术后病理检查提示:新辅助化疗后子宫颈仍可见癌灶残存;癌灶累及子宫颈1~4点和6~12点,浸润最深处<1/3子宫颈厚度;癌细胞退变明显,间质多量淋巴细胞、浆细胞及泡沫细胞增殖,局部纤维组织增生( 图1D , 2D ),符合化疗后反应,残存癌组织约占30%;子宫体未见明确癌灶累及;可见脉管内癌栓,未见明确神经侵犯现象;左侧盆腔淋巴结可见癌转移(2/9),右侧盆腔淋巴结可见癌转移(1/4),余淋巴结未见癌转移(0/5)。免疫组化检测显示,p16、CK7、CK5/6阳性,Ki-67阳性比例约80%,p53突变型(弥漫阳性),符合HPV感染相关性子宫颈ISMC。见 图4 。术后诊断:子宫颈癌(ISMC亚型),Ⅲc1r期,新辅助化疗后。经过多学科团队讨论,考虑患者的肿瘤细胞中细胞程序性死亡受体1(programmed cell death protein ligand 1,PD-L1)阳性比例为40%,根据2022年美国国立综合癌症网络(National Comprehensive Cancer Network,NCCN)指南 [ 1 ] ,患者目前存在以下高危因素:淋巴结转移、脉管内癌栓,建议予白蛋白紫杉醇+卡铂方案化疗联合PD-L1抑制剂卡度尼利单抗治疗2个疗程后行放疗,放疗后继续化疗4个疗程。治疗后规律随访34个月,无复发征象。
讨论
子宫颈ISMC是HPV感染相关性子宫颈腺癌,具有表型可塑性和侵袭性生物学行为 [ 2 ] 。与其他HPV相关性子宫颈腺癌亚型相比,ISMC更早发生淋巴脉管浸润和淋巴结转移,预后更差。
1. 发病机制:2016年,Lastra等 [ 3 ] 发现子宫颈ISMC可能比常见的HPV相关性子宫颈腺癌更具侵袭性。2020年WHO女性生殖系统器官肿瘤分类 [ 4 ] 将ISMC归入HPV感染相关性子宫颈腺癌,该病理亚型通常为HPV 18型感染所致,生物学特性为侵袭性,预后差于普通子宫颈腺癌。
2. 形态学特征:子宫颈ISMC的肿瘤细胞呈复层排列,与普通子宫颈腺癌的单层或假复层排列不同,在癌巢中可见多排癌细胞相互叠加;癌巢的周边癌细胞常呈栅栏状排列,这一特征有助于在显微镜下对该肿瘤进行识别。
子宫颈ISMC的癌细胞形态为柱状或立方状,细胞质内含丰富黏液,与正常子宫颈黏液细胞具有一定相似性,但细胞大小及细胞核存在明显的异型性 [ 5 ] ,表现为细胞大小不一,细胞核形态不规则,核质比增大等,异型性细胞核常位于细胞的基底部;与正常细胞的细胞核相比,ISMC细胞的细胞核更大、形状更不规则,染色质也更加粗糙、深染。肿瘤组织结构可形成复杂的腺样结构,类似于正常腺体,但形态往往不规则;腺腔的大小和形状各异,腺腔内可充满黏液 [ 6 ] ;还可形成筛状结构,即细胞之间通过桥粒等连接形成类似筛孔的结构,黏液可积聚在这些筛孔样的间隙中 [ 7 ] ;部分肿瘤区域可呈实性巢状结构,细胞紧密排列,几乎没有腺腔形成,在实性巢状结构内癌细胞仍然保持复层排列的特点。
本文报道的例1子宫颈ISMC患者,常规病理检查可见癌巢内癌细胞排列紧密,呈栅栏状,癌巢内可见散在及灶性分布的产黏液细胞,部分细胞的细胞质透亮,提示黏液丰富,可见明显Silva C型表现,右侧肿瘤腺体向左侧弥漫性浸润。但子宫颈ISMC的肿瘤结构具有多样性,如岛状、腔状、实心、乳头状、小梁状、微乳头状、单细胞浸润结构,以及不同的癌细胞形态,可表现为嗜酸细胞质、细胞质透明、玻璃样细胞、环样信号(肿瘤细胞成环状透亮,胞质出现环状分布的黏液空泡)、奇异细胞核、鳞状分化等特征。
3. 免疫表型:免疫表型特征有助于子宫颈ISMC的鉴别,主要包括以下3个方面:(1)肿瘤细胞(包括单纯ISMC、混合性ISMC及复层产黏液上皮内病变)均为p16弥漫阳性表达且Ki-67高表达(阳性比例为50%~90%) [ 8 ] 。本文报道的2例子宫颈ISMC患者的免疫组化检测结果均表现为p16弥漫性阳性表达且Ki-67高表达。但仅根据p16阳性不足以诊断ISMC,因为在子宫颈ISMC和浆液性癌中p16通常均呈弥漫强阳性。(2)需关注CK5/6和CK7表达的异质性,普通子宫颈腺癌常存在CK7的弥漫强阳性表达、CK5/6阴性表达,而ISMC巢状肿瘤细胞周边的基底样细胞常表现为局灶区域p40及CK5/6阳性。(3)子宫颈ISMC的生物学特性凶险,具有高侵袭性病理特征(如:深浸润、淋巴脉管浸润、淋巴结转移),可能是部分累加p53突变效应导致。p53突变型表达的免疫组化染色呈弥漫阳性或全阴性,本文报道的2例子宫颈ISMC患者的免疫组化检测结果均为p53突变型(例1为p53全阴性,例2为p53弥漫阳性)。有研究报道,子宫颈ISMC患者大多数显示了p16的块状阳性,而CK5/6则是斑点状阳性,或完全阴性 [ 9 ] 。
综上,子宫颈ISMC的p16、Ki-67呈弥漫阳性表达,p53为突变型,CK5/6呈局灶区域阳性表达。如果p16和Ki-67免疫组化染色为阳性可以排除良性病变。
4. 鉴别诊断:子宫颈ISMC应与鳞癌、腺癌及腺鳞癌相鉴别。子宫颈鳞癌常表现为外生型或溃疡性肿块,质脆易出血;镜下观察,癌细胞排列成巢团状,可见角化珠、细胞间桥,间质反应(即促纤维增生)明显。子宫颈腺癌镜下观察显示,癌细胞通常排列成腺管状,黏液分泌相对较少且分布较均匀,细胞形态较为单一,多为柱状细胞,细胞核的异型性相对一致,没有ISMC那样明显的复层排列和周边栅栏状结构。免疫组化检测显示,子宫颈腺癌细胞p16一般呈弥漫强阳性,雌激素受体(ER)、孕激素受体(PR)可呈阳性表达,尤其是在一些分化较好的普通型子宫颈腺癌中;而子宫颈ISMC细胞p16通常弥漫阳性表达,但部分患者可出现p16表达缺失或减弱,ER、PR通常为阴性表达。子宫颈腺鳞癌具有腺癌和鳞癌两种成分,镜下观察可见明确的鳞癌区域,如癌细胞有角化、细胞间桥等鳞状细胞的特征,同时存在腺性分化区域,两种成分之间可有移行过渡。免疫组化检测显示,鳞癌区域p63、p40等鳞癌标志物呈阳性,而腺癌区域表达腺上皮标志物,两种成分通过免疫组化检测可以明确区分。子宫颈ISMC主要由产黏液的腺上皮细胞组成,虽然细胞有异型性,但仍以腺性分化为主,鳞状分化成分极少或无;免疫组化方面表达腺上皮相关的标志物,如癌胚抗原(CEA)等呈阳性,而鳞癌标志物(如p63、p40等)通常为阴性或仅少量散在阳性。
此外,子宫颈ISMC还应与黏液表皮样癌鉴别。原发性子宫颈黏液表皮样癌罕见,镜下观察可见表皮样细胞、黏液细胞和中间细胞3种特征性细胞,具有鳞状分化,但无相应的上皮内病变,且病灶内无中性粒细胞浸润,细胞凋亡不显著。产黏液细胞常位于癌巢中央,为杯状细胞或印戒样细胞,过碘酸雪夫反应(PAS)染色阳性,且CEA阳性,波形蛋白(vimentin)阴性,可与ISMC鉴别。
5. 治疗及预后:子宫颈ISMC较其他HPV感染相关性浸润癌的预后更差,更易产生化疗耐药。近年来,也有研究报道高级别鳞状上皮内病变(high-grade squamous intraepithelial lesion,HSIL)可与ISMC并存 [ 10 ] ,分子遗传学检测和PD-L1检测可为临床提供更多靶向及免疫治疗相关信息 [ 11 , 12 ] 。子宫颈ISMC患者的中位发病年龄为43岁,与普通子宫颈癌患者的发病年龄相似。大部分子宫颈ISMC的肿瘤最大径>2 cm,外观呈息肉状外翻 [ 13 ] 。Horn等 [ 14 ] 报道的11例子宫颈ISMC患者中,7例平均在7.8个月后复发,5例出现远处转移(其中3例为肺转移)。本文报道的2例子宫颈ISMC患者虽为局部晚期,但通过免举宫器的机器人系统辅助下腹腔镜手术,减少了手术创伤,避免了放疗可能带来的一系列并发症,规律随访至今34个月均未复发,预后良好。这2例患者年龄<45岁,手术治疗保留了阴道,提高了生命质量。对于局部晚期的子宫颈癌患者,如果患者要求行腹腔镜手术切除,充分评估后可由资深妇瘤医师进行手术,术中免举宫器操作,行子宫悬吊辅助手术,并严格进行无瘤操作,可减少手术创伤、加速术后康复。
综上,子宫颈ISMC是具有侵袭性生物学行为、恶性程度较高的腺癌,中~低分化,Sliva C型;其淋巴脉管浸润、淋巴结转移早,且易产生化疗耐药。子宫颈ISMC细胞中PD-L1高表达,可考虑联合PD-L1抑制剂免疫治疗。子宫颈ISMC患者的预后差于普通子宫颈腺癌,需加强对其规范治疗及密切随访。本文报道的2例患者出现阴道流血症状后进行活检病理检查,明确ISMC诊断后,行改良的机器人系统辅助下腹腔镜子宫颈癌根治性手术,术后经多学科团队讨论后给予补充放化疗,目前已密切随访34个月未复发,显示预后良好。后续将积累更多的病例并延长随访时间,更深入地认识本病并规范诊治。



